眼看着新冠疫情已经进入第三个年头了,记得那个时候病毒已经在美国和欧洲的大城市悄悄地传播,大家全都盯着武汉捐钱捐口罩,CDC测试搞不出来两眼一抹黑,天天在那里”the risk is very very low”安慰大家。
两年时间新冠病毒的优势毒株已经最早期的wuhan strain变成2020年春季出现的D614G,再变成alpha,然后是delta,最近又变成omicron,总共换了四次。这两年来人类对新冠病毒,covid病理,免疫,药物,病毒突变等等都有了很深的了解,但是面对这样一个快速突变的病毒,我们仍然有一些不完全了解的东西。这里面有一些是known unknowns,我们知道我们不知道;还有一些unknown unknowns,我们不知道我们不知道。
这篇科普文章参考了很多最近的paper和preprint,简单总结一下关于新冠病毒,long covid,和疫苗/药物/口罩的一些新的研究结果,时间关系不可能一个个找出处。不喜欢看的请点左上角小叉号,我有个长长的屏蔽名单,嘴上不干净的我基本上都屏蔽了,反正你们说啥我也看不见~~
1,病毒
Omicron出来以前我对疫情一直是比较乐观的,因为即使突变的最厉害的beta也没有逃出疫苗的免疫,去年夏天出现的delta凭着更高的病毒量和更短的潜伏期能够造成一些突破感染,但是突变的其实不算厉害,第三针一打又恢复了90%+的有效率。新冠病毒作为一个单链RNA病毒当然随时在突变,但是在正常人群里面传播的时候形成一个新毒株其实不是那么容易的事情。如果把病毒的fitness level比作地形,海拔越高相当于越fit的话,老的毒株就好比已经在一个小山包上,周围当然可能还有更高的山峰。如果病毒想要靠突变爬上周围更高的山坡的话,难免要经过一些山谷,但是山谷里面的病毒突变fitness不够,很容易被别的毒株给竞争掉。所以在D614G出现大半年之后,才冒出来了第一个真正有竞争优势的alpha变种;印度靠着14亿人和很高的人口密度,才培养出了delta。不管是alpha, beta, delta还是lambda,都远远没有逃出疫苗和自然感染能够保护的范围。
但是这次Omicron的横空出世告诉我们一个事情,病毒除了正常的突变,还可以在山谷里架桥直接爬上更高的山头。这个桥梁有两种,一个是艾滋病人的long infection,另一个就是传给动物然后回传给人类。现在一般认为Omicron能够出现,和这两个因素可能都有关系。新冠病毒有了艾滋病人和动物回传这两个大招以后,Omicron很可能不是唯一一个能够几乎完全逃逸对上一代毒株的免疫几周内横扫全球的新突变。我觉得这次Omicron的症状比较轻并不是必然的,只是人类比较幸运,下一次会不会还这么幸运呢?
Omicron让我们知道了新冠病毒还有这两个非常厉害的大招,那么新冠病毒突变的极限到底在哪里呢?下一个突变能在多大程度上逃逸疫苗和以往感染的保护?有没有能力突变到可以结合别的受体直接搞出SARS3来?这些事情我们并不清楚。Omicron wave对疫苗率很高的国家/地区来说杀伤力有限,这一波过后各国纷纷取消限制进入endemic状态,但是人类和新冠病毒的战争还有很长的路要走,下一代疫苗,抗病毒药物,变种检测,还有对long covid的研究都一定要跟上。
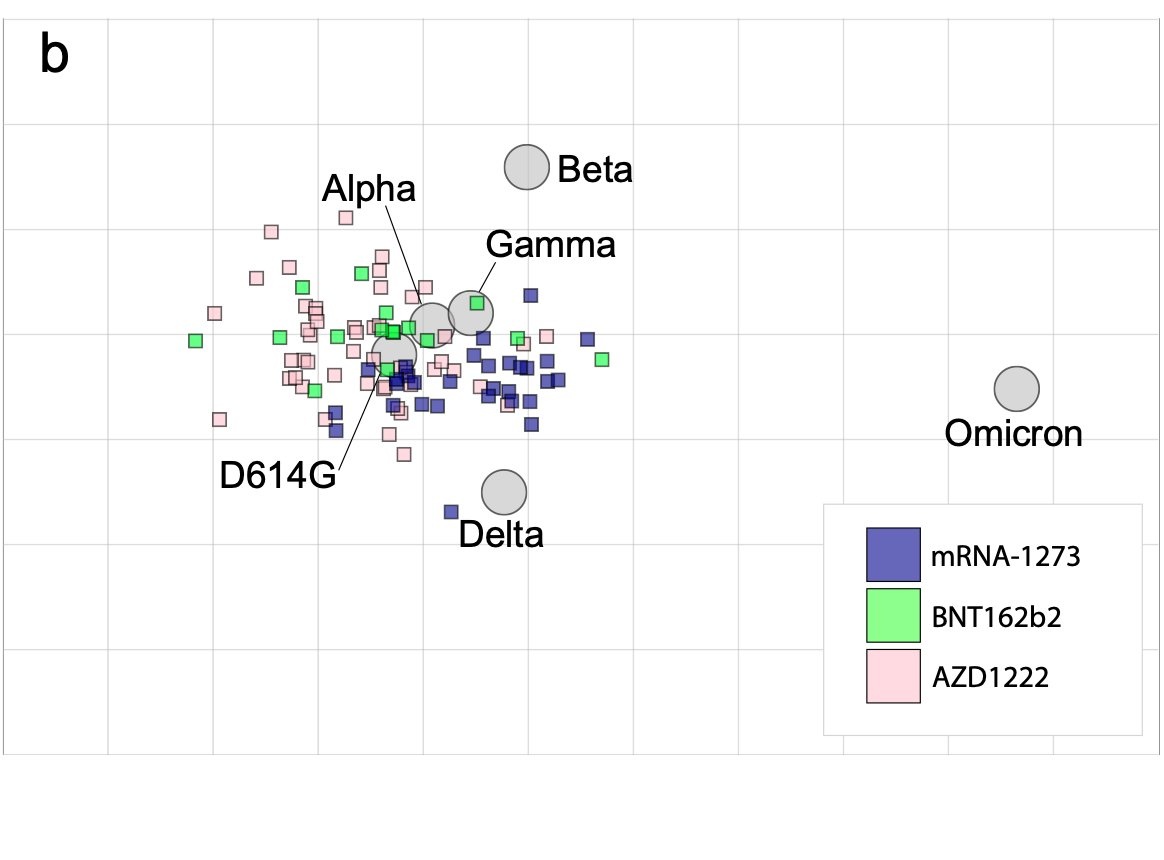
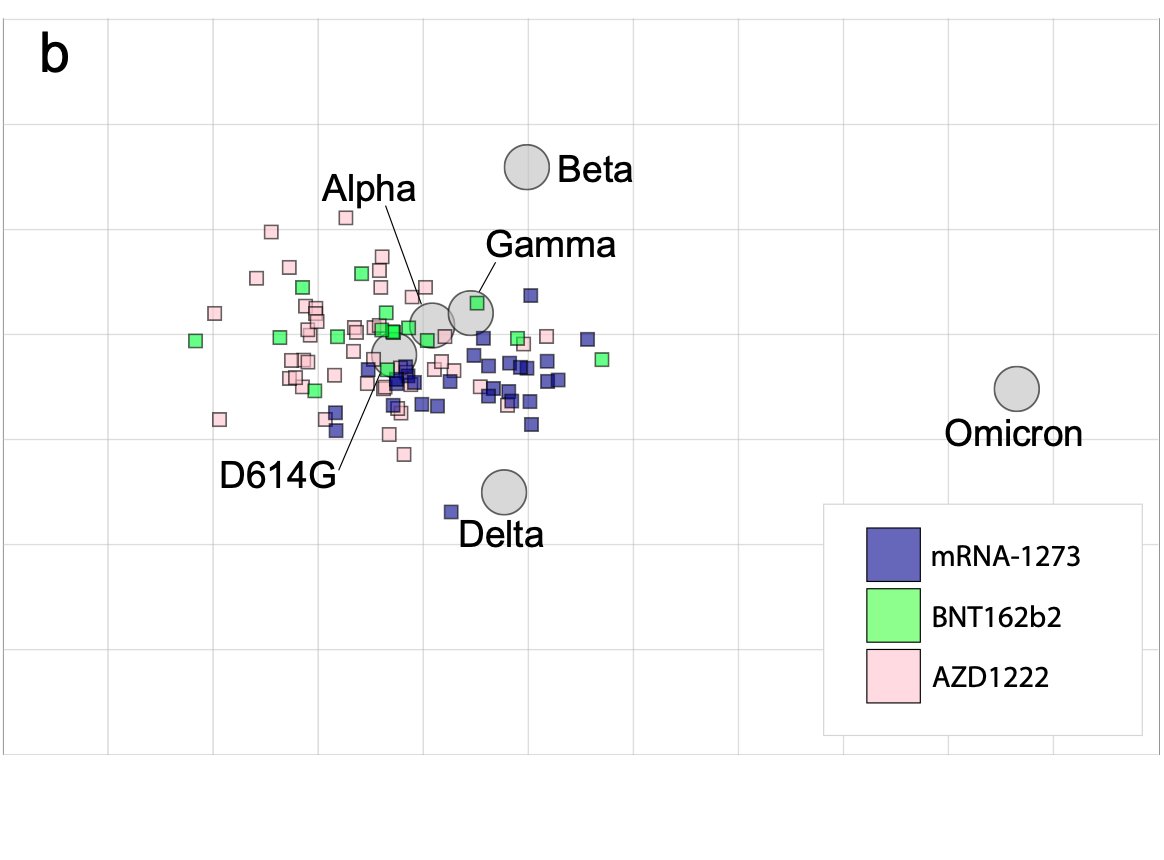
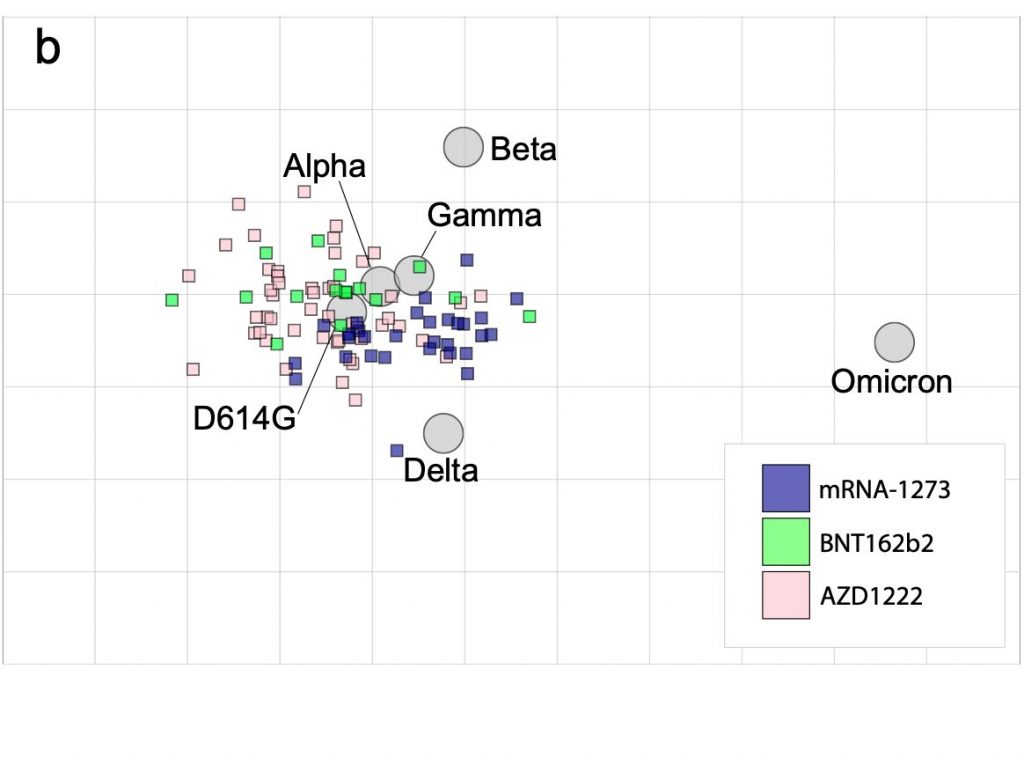
贴一张图,各个变种以及疫苗从免疫角度来看的大概位置,可以看到这个Omicron突变的有多么厉害,离疫苗能够高效覆盖的范围有多远。
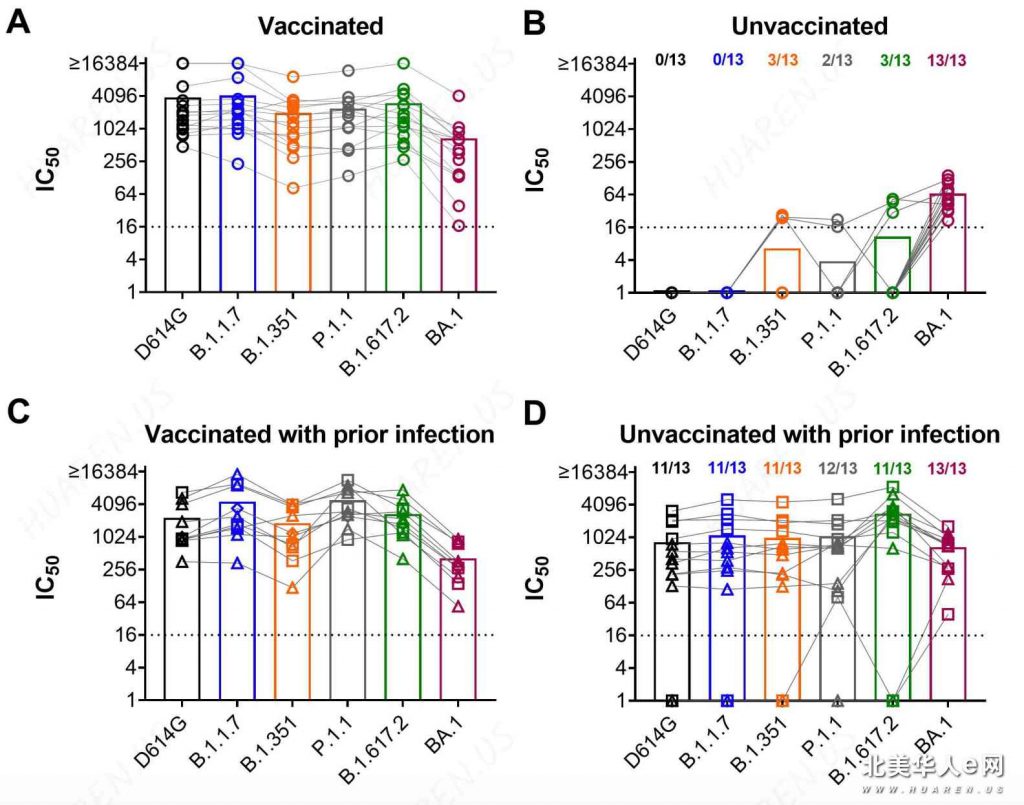
最后,对于Omicron本身我们其实也有一些不清楚的东西。比如说连续有好几个研究都发现,Omicron症状不严重,但是产生的免疫力相对也比较低。对于没打过疫苗的人来说,感染过Omicron以后不光对其他毒株保护力非常低,对Omicron本身也不高。对打过疫苗的人来说,感染Omicron以后对Omicron的滴度也明显小于对其他毒株的滴度。(看下面的图)Moderna/NIH最新的动物实验也发现Omicron specific的疫苗和原版的疫苗第三针比起来好像并没有什么优势,打完Omicron specific的第三针以后,能够对同时对wild type和Omicron有反应的B细胞比例高于原版疫苗的第三针,但是这并没有转化成更高的中和滴度。不过这个是猴子的实验,不能过分解读。这个现象和immune imprinting有关,但是有可能和Omicron spike本身的免疫原性也是有一定关系的。
注意这里我用的是immune imprinting而不是所谓的original antigenic sin,因为感染omicron以后或者第三针以后确实是能够生成对omicron的抗体的,而且抗体水平还不低,大概相当于两针疫苗对wild type的水平,不是说打了原版疫苗或者感染过老毒株就对omicron产生不了免疫力了,不应该叫”sin”。但是由于感染omicron以后被唤醒的是前两针疫苗生成的记忆B细胞,这些记忆B细胞经过几轮分化和选择以后,最后选出来的大部分是能够同时识别wildtype和omicron的B细胞,所以感染Omicron以后对其他毒株的抗体水平也有了明显的上升,就好像带着原版疫苗/毒株形成的imprint一样。
2,PACS(也就是long covid)
其实这是我写这个帖子的主要目的,最近有很多对long covid的研究都有了文章或者preprint,目前人类对long covid不了解的地方当然还有很多,但是已经不是什么都不清楚的状态了。Omicron wave过后我相信政府层面的各种restriction会很快取消,大家都准备live with the virus。但是作为个人来讲,我并不主张完全躺平,因为long covid的危害我们至今都不是完全清楚。如果没有其他的risk factor的话,经过各种疫苗和感染的组合以后新冠重症的概率是很小的,但是新冠病毒轻症仍然有一定的概率会引发long covid,而有一些long covid可能会给生活质量带来极大的影响。今后在相当长的一段时间内,我个人在室内环境肯定还是会戴好KN95。
首先long covid到底是怎么回事呢?现在肯定不能说每一种long covid的机制都清楚,但是一般认为long covid有以下几种可能:1,病毒通过嗅神经进入大脑直接感染神经系统,2,血栓特别是微血栓,3,cytokine(细胞因子)水平异常触发炎性反应,4,自免疫。新冠病毒并不是一个嗜神经的病毒,直接感染大脑的例子确实有,但不是很多。但是一旦病毒进入大脑开始感染脑细胞的话,后果可能会极为严重,有证据证明这样的long covid可以是degenerative的,大脑会出现类似于老年痴呆症的改变,比如beta淀粉样蛋白聚集,神经系统出现炎性反应等等。比如下面的文章里面研究了五个这样的病例。
https://www.biorxiv.org/content/10.1101/2022.01.31.478476v1.full.pdf
long covid的另一个可能来源是所谓的血栓,新冠是一个血管疾病其实已经不是什么新闻了,重症新冠会造成血管内皮的严重损害,接下来就是血栓高发,现在医院基本上都知道要给新冠住院病人用抗凝药了。但是有一些研究发现轻症新冠也可以引起一定的凝血异常,血液里面会出现大量的microclots,比如下面这篇文章。当然这篇文章的研究做的比较粗糙,只是找了70个long covid病人验血发现有microclots,然后给其中的24人吃抗凝药发现他们症状有好转,并没有和没有long covid症状的健康人做对照。所以现在只能说microclots *有可能*能够解释一部分long covid,不能像一些贩卖焦虑的自媒体那样一口咬定long covid都是凝血问题。
https://assets.researchsquare.com/files/rs-1205453/v1_covered.pdf?c=1640805028
前几天耶鲁大学的Akiko Iwasaki和Stanford的Michelle Monje联合发表了一篇重磅文章,提出相当一部分long covid可能是因为异常的cytokine(细胞因子)水平激活了小胶质细胞(一种神经系统的免疫细胞),导致了神经系统的炎性反应,这个机制和化疗病人出现brain fog类似。这是一个非常重要的发现,解释了为什么病毒不需要直接进入大脑就可以引起大量的神经系统症状。另外还有文章发现一些新冠康复病人的肺部会有长期活跃的杀手T细胞攻击自己的正常细胞,引起局部的炎性反应,这种反应会持续一年左右直到呼吸道的损伤被完全修复。一个很奇怪的问题是,为什么这种异常的细胞因子水平和T细胞水平能够持续这么久呢?最近几篇关于long covid的文章里面给了几种猜测,一是可能体内还有没有被清除掉的病毒碎片还在刺激免疫系统;二是组织修复的时候产生的细胞因子可能延长了相关免疫细胞的寿命;三是自免疫,细胞因子水平异常可能是体内有能够结合细胞因子的自免疫抗体,T细胞水平异常可能这些T细胞识别的都是自身的抗原。
这几种猜测里面我个人其实比较倾向于第一种可能,因为连续有几个对记忆B细胞的研究都发现,随着时间的增长,自然感染产生的记忆B细胞不光产生抗体的亲和力增加,结合位点的广度也有明显提高;而疫苗产生的记忆B细胞结合位点的广度增加有限,主要是增加抗体对已有结合位点的亲和力,这个现象是感染+疫苗产生super immunity的理论基础。但是为什么自然感染后好几个月记忆B细胞结合位点的广度还在不断增加呢?一个很可能的原因就是体内其实还有一些病毒碎片起到了抗原的作用能够继续刺激免疫系统。这个现象对免疫来说当然是好事,但是对于long covid患者来说,可能是一件非常糟糕的事情。
https://www.biorxiv.org/content/10.1101/2022.01.07.475453v1.full.pdf
nature.com/articles/s41590-021-01104-y.pdf
最后一个可能就是自免疫,我们早就知道新冠,特别是重症新冠是可以产生大量自免疫抗体的,很多自免疫抗体针对的就是自己的各种细胞因子。那么有没有可能Akiko她们观察到的细胞因子异常就是这么来的呢?这些自免疫抗体还能够造成什么别的损害?这个问题我们其实还不完全清楚。但是我们从对其他病毒的研究中知道,病毒通过影响免疫系统造成长期严重后遗症的例子是很多的,比如最近有一项研究基本上实锤了EBV病毒和多发性硬化的关系,EBV是个急性期症状普遍轻微的病毒,但是这个病毒可以潜伏在人体的免疫细胞内,后患无穷,最近发现连一些long covid都可能和EBV感染有密切关系。
另一个问题是,疫苗到底能够减少多少long covid呢?一般的说法是疫苗大概能够把long covid的比例降低一半。但是这里有一个问题就是long covid症状多种多样,没感染过新冠的人一样会有头疼疲惫之类的“症状”。以色列有一个最新的研究比较了打过疫苗和没打过疫苗的新冠康复者,以及未感染人群中间出现各种的long covid症状的比例,发现新冠康复者出现各种long covid症状的概率大概是未感染者的2倍,但是打过疫苗的康复者和未感染者出现long covid症状的概率在统计上看不出显著区别。当然这个研究的规模不够大,置信区间很宽,不能太把这些数字当回事。我认为我们得到的结论应该是:1,新冠重症很可怕,但是新冠轻症long covid的问题没有一些中文自媒体宣传的“一半的新冠幸存者有后遗症”那么可怕,虽然新冠轻症后出现各种long covid症状的概率确实明显高于未感染者;2,疫苗能够减少long covid症状出现的概率,但是并不能完全避免,能够不感染新冠尽量还是不要感染。
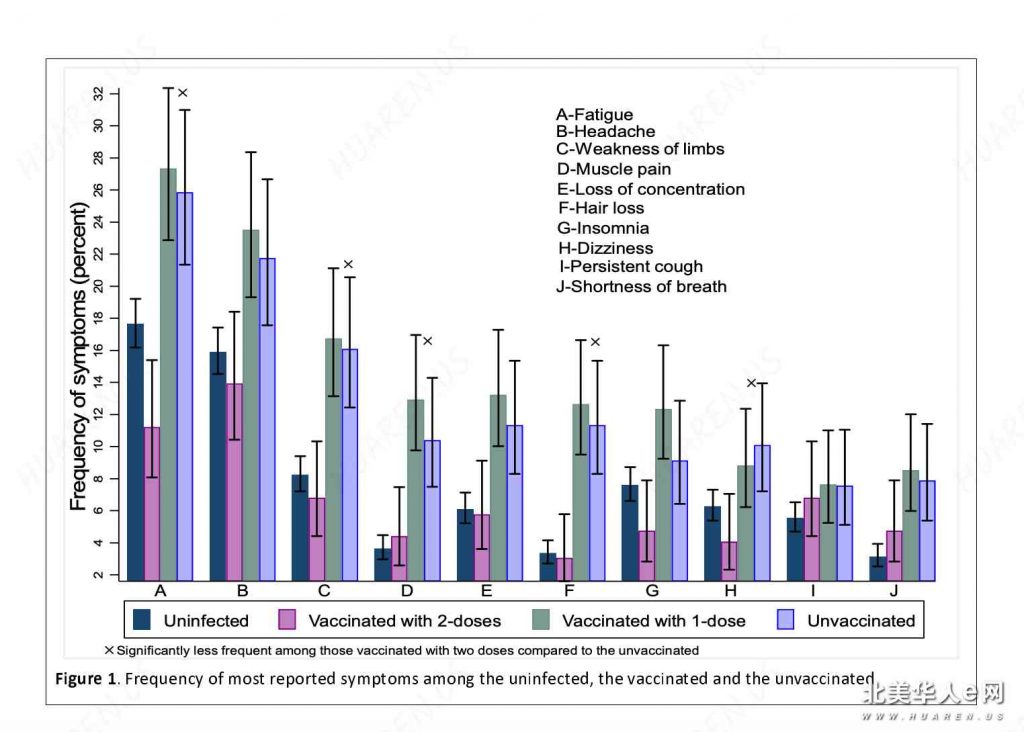
3,疫苗、药物、口罩
首先贴一张图,疫苗在2021年到底避免了美国境内的多少新冠死亡?这里的估算大概是110万。新冠疫苗在alpha和delta这两波疫情中减少了大量的损失,由于alpha变种对疫苗几乎没有逃逸能力,我们去年几乎没有看到alpha wave的影响。delta有一些逃逸能力,但是疫苗仍旧避免了大量的感染、重症和死亡,特别是在疫苗率很高的一些蓝州。和疫苗在2021年避免的巨大损失相比,疫苗的造成的损失和风险都是很小的。
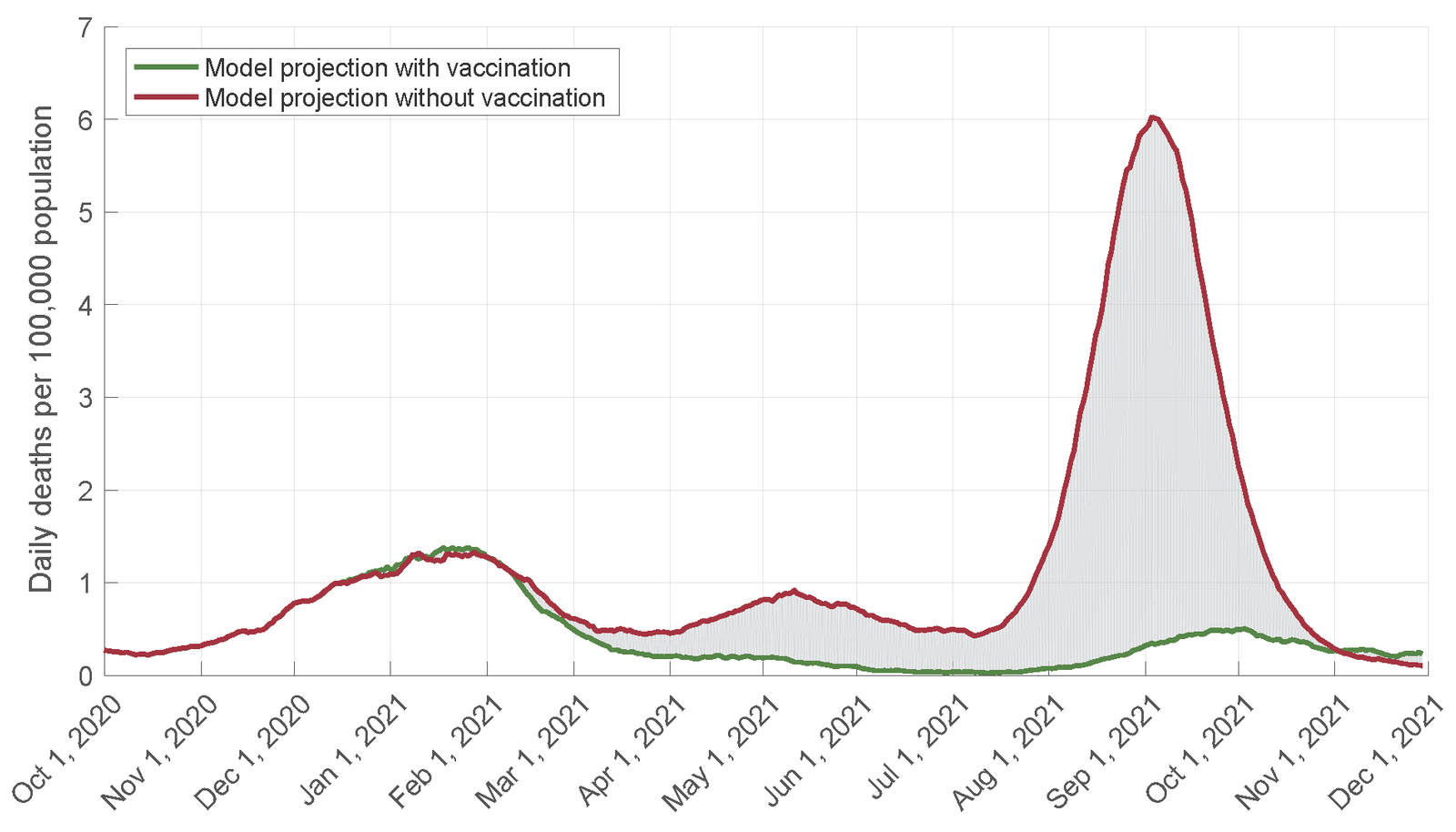
但是另一方面,现在是2022年2月,整个新冠疫情的形势有了很大的不一样。一方面新冠病毒已经进化了好几代了,新的omicron虽然症状轻,但是对疫苗的逃逸非常厉害,三针疫苗能够减少一些感染,两针几乎减少不了感染。当然由于T细胞还能很好地识别omicron,打了疫苗仍然重症的例子主要集中在免疫力比较差的高龄人群中。另一个很重要的变化就是现在covid naive的人已经很少很少了,Omicron wave过后,大多数人都经历了疫苗和感染的某种组合,免疫系统实实在在的见过了至少一次进入细胞内的新冠抗原。由于这两个变化,2021年的很多应对疫情的策略已经很明显的过时了。
先说一下现有疫苗的两个短板:现在人们对mRNA疫苗和自然感染产生的免疫反应已经研究的很深了,mRNA疫苗的好处是最大限度的模拟真实感染,用自己的细胞去合成抗原,然后这个细胞(一般是肌肉细胞和周围淋巴结的细胞)就会把抗原-MHC1复合物挂在外面,同时分泌干扰素报警,等着APC过来呈递抗原。最后这个被“感染”的细胞会被CD8+ T细胞给杀死。这个过程从免疫系统的角度来看和真实感染非常接近,因此产生的细胞免疫和免疫记忆是细胞外抗原的疫苗(灭活/重组蛋白)很难比较的。但是疫苗和自然感染过分接近的问题就是炎性反应比较重,免疫系统激活牵扯到一系列细胞因子的释放和信号通路的激活,这种upregulation在有些人身上会引发一些downstream的严重不良反应,比如心肌炎。很多人抱怨的打完疫苗后皮疹,心悸,头痛等等很可能也是和这个有关。炎性反应重应该是mRNA苗和腺病毒疫苗的通病,当然腺病毒疫苗还有一些自己独有的问题,可以理解为劣化的mRNA疫苗。第二个短板就是疫苗诱导的粘膜免疫不足,特别是和自然感染比起来。这个问题在开发疫苗的wild type时代不是很严重,因为那个时候新冠的潜伏期很长免疫系统来得及反应。但是现在Omicron的潜伏期只有3天左右,要想避免有症状感染和病毒的进一步传播,基本上只能靠鼻粘膜里面已有的抗体。而肌肉注射的灭活疫苗完全产生不了粘膜IgA,mRNA疫苗也只能产生很少的粘膜IgA,大部分都要靠血液里的IgG扩散过去,其实效率很低的。相比之下肺部是血清IgG的主战场,所以疫苗对重症的保护能力一直都不差,不管是什么变种。
在大部分人都没有接触过新冠抗原的时候,mRNA疫苗的收益明显大于风险,强大的细胞免疫也是重组蛋白疫苗和灭活疫苗很难相比的。但是现在大家的免疫系统基本都见过这个病毒,重症的风险已经变小了很多。由于免疫记忆的存在,细胞外抗原(重组蛋白)在细胞免疫上的劣势也变小了。(举个例子,流感是大家都见过无数遍的病毒,这个时候mRNA疫苗的效果其实还不如无佐剂的简单灭活。)这个时候我认为FDA应该给人们更多的选择,如果有一些高危因素需要打booster,同时又已知自己对mRNA疫苗反应很大的话,应该给这些人一个选择其他种类的疫苗的可能,比如Novavax。在Novavax之外,其实我还有两个比较看好的方案,一个是下面这篇文章里面的魔改版灭活,灭活的不是新冠病毒(因为直接灭活无法把spike protein固定在prefusion状态),而是在NDV(新城疫病毒)上面表达的一个叫做HexaPro的刺蛋白超稳定构型。这个疫苗是在鸡胚里面培养的,培养完以后灭活提纯,从头到尾完全是成熟技术,抗体水平高于康复患者,同时生成的大部分抗体都是有效的中和抗体,看起来非常promising。二是Akiko组提出的方案:不需要为了粘膜免疫单独做一个鼻喷减活或者腺病毒疫苗,肌肉注射mRNA疫苗两周后往鼻粘膜里面喷一次spike protein就可以。具体细节看下面的这个twitter thread。
https://www.medrxiv.org/content/10.1101/2022.01.25.22269808v1.full.pdf
Vaccines that reduce infection & disease are needed to combat the pandemic. Here, @tianyangmao @BenIsraelow et al. describe our new mucosal booster strategy, Prime and Spike, to induce such immunity via nasal delivery of unadjuvanted spike vaccine ? (1/)https://t.co/J4NuUgiI7e pic.twitter.com/bcB5MFph9F
— Prof. Akiko Iwasaki (@VirusesImmunity) January 27, 2022
由于新冠病毒快速突变的特性,疫苗之外治疗手段也是很重要的。目前最好的早期治疗药物基本上就是对Omicron仍然有用的GSK单抗和口服药Paxlovid,Merck的molnupiravir产量更大,但是有更多的safety concern和引起病毒突变的concern,其实我个人对Merck把这个药outsource给一大堆第三世界国家随便生产是非常担心的。单抗和Paxlovid的有效率当然很高,但是至少在未来的几个月内,Paxlovid只会被用在高危人群身上,因此已有药物的repurposing仍然有意义。
现在已有常用药物里面唯一一个在大规模RCT里面做出正面结果来的是一个叫做fluvoxamine的抗抑郁药物,不过至少在目前,NIH给的guideline仍然认为加拿大TOGETHER trial给的证据还不够充分。然后被政治化很厉害的神药/马药Ivermectin有很多正反两面的anecdotal data,但是在包括加拿大TOGETHER在内的几个大规模RCT里面表现普遍不好,再加上有四五个第三世界国家结果too good to be true的小规模trial造假被抓包。不管怎么样,Fluvoxamine和Ivermectin这两个药还有一个叫做Fluticasone的哮喘药物现在都在等着NIH的ACTIV-6 trial盖棺定论。有一些说法是这个月或者下个月ACTIV-6可能会报告一些中期结果,我个人认为fluvoxamine在这三个常用药物里面的希望是最大的。
最后是口罩,只贴一张图,CDC前两天通过1800多个case match做出来的口罩有效率,虽然不是随机双盲对照的RCT(显然口罩是无法双盲的),但毕竟是个真实世界中做出来的结果,比我两个月前贴的那个流体力学simulation的文章有说服力得多。CDC的反射弧特别的长,从疫情开始到现在所有的事情都慢好几拍,想象一下这个结果如果出现在2020年2月的话,能够减少多少不必要的新冠死亡和重症?新冠疫情的变化非常快,一个新冠病毒的新变种几周的时间就能横扫全球。在这个时候,作为政府/FDA/CDC,决策up to date非常重要,昨天有用的东西拿到今天很可能就过时了。很不幸,和病毒的速度相比,美国的政府机构,特别是CDC,可以说反应是非常迟缓的。